臨床試験の概要
- 臨床試験の目的
-
腎細胞がんに対する治療を休止することの意義を評価する臨床試験※です。
臨床試験とは、患者さんに参加・協力していただいて治療法や診断法の有効性や安全性を調べる研究のことをいいます。現在行われている多くの治療法や診断法も、国内および海外で行われた臨床試験によって進歩してきました。
この臨床試験は、新しい薬(未承認薬)の厚生労働省による承認を得るために、主に製薬企業が主体となって行う「治験」とは異なり、研究者(医師)が主体となって行う研究者主導臨床試験であり、 JCOG(ジェイコグ)※という多施設共同臨床試験グループにより行われます。JCOG(Japan Clinical Oncology Group):日本臨床腫瘍研究グループ
- 臨床試験の対象となる方
-
腎細胞がんと診断され、
「ニボルマブ」、「ペムブロリズマブ+アキシチニブ」、
「アベルマブ+アキシチニブ」、「ニボルマブ+カボザンチニブ」、
「ペムブロリズマブ+レンバチニブ」による
治療を半年以上継続して受けている
(治療によってがんが小さくなり病状が半年以上安定している)、
登録日の年齢が20歳以上の患者さん※さらに詳細な対象につきましては、別途お問合せください
- 登録数と研究期間
-
予定登録患者数 250人 期間 予定登録期間:5年。追跡期間:登録終了後4年。解析期間:1年。総研究期間:10年 臨床研究の開始予定日 2020年7月20日 臨床研究の終了予定日 2030年7月19日
- 臨床試験参加へのご相談・お問合せはこちら
-
資料のダウンロードはこちら
本臨床試験紹介資料ダウンロード
本臨床試験の概要
免疫チェックポイント阻害薬による治療
臨床試験は、腎細胞がんと診断され、「ニボルマブ」、「ペムブロリズマブ+アキシチニブ」、「アベルマブ+アキシチニブ」、「ニボルマブ+カボザンチニブ」、「ペムブロリズマブ+レンバチニブ」のいずれかによる治療を半年以上継続して受けている(治療によってがんが小さくなり病状が半年以上安定している)患者さんを対象としています。
現在治療を受けられている「ニボルマブ」、「ペムブロリズマブ」、「アベルマブ」はいずれも、免疫チェックポイント阻害薬※1と呼ばれる薬で、特にその働きから「PD-1経路阻害薬」に分類されています。
免疫チェックポイント阻害薬以外の多くの抗がん薬では、治療を中断すると病状は悪化してしまうため治療は継続して行うことが一般的です。免疫チェックポイント阻害薬によってがんが小さくなり、半年以上病状が安定している患者さんに対しても、引き続き同じ薬剤での治療を続けることが標準治療ですが、最近になり、がん細胞を攻撃する力(免疫機能)は、副作用などによって免疫チェックポイント阻害薬を中止した後も持続することがあることがわかってきました。
※1 免疫チェックポイント阻害薬
免疫機能が正常に働いている状態では、免疫細胞(特にT細胞)が、がん細胞を認識してがん細胞を攻撃します。しかし、多くのがん細胞は、免疫細胞の働きにブレーキをかける仕組みを持っており、免疫細胞の攻撃から逃れて、身体の中で増殖します。免疫チェックポイント阻害薬は「がん細胞がT細胞のブレーキを踏まないようにする」ことで、免疫細胞が本来の機能を回復してがん細胞を攻撃できるようにします。免疫チェックポイント阻害薬には、作用する部位によっていくつかの種類があります。腎細胞がんの治療に用いられる免疫チェックポイント阻害薬にはニボルマブとペムブロリズマブがあります。
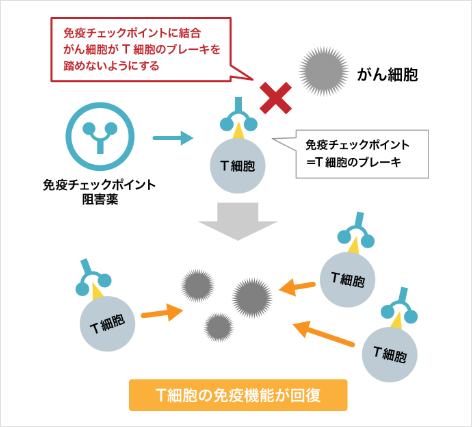
免疫チェックポイント阻害薬の働き(イメージ)
当臨床試験の意義
免疫チェックポイント阻害薬を半年以上継続して受けると、免疫チェックポイント阻害薬により、がん細胞を攻撃する力が高まって、がん細胞が排除されたり、がんの進行が抑えられていると考えられます。そのため、免疫チェックポイント阻害薬の治療を長期に連続して受けなくても、効果が持続する可能性があると考えられます。
そこで、免疫機能が半年以上安定的に働き、免疫チェックポイント阻害薬の治療中の患者さんであれば、意図的に治療をいったん休止しても治療効果は持続するのではないかと考え、この臨床試験を行うことになりました。
また、治療をお休みすることで、治療を続けることで発生する有害事象(6 か月で15%、その後も1 年に5~10%の患者さんに重い副作用が見られます)を回避したり、医療費を節約したりすることができます。

臨床試験の治療法について
臨床試験では、以下のA群かB群のいずれかの治療を受けていただきます。
- A群(標準治療)
- 現在受けている免疫チェックポイント阻害薬(ニボルマブ、ペムブロリズマブアベルマブ、アベルマブ)の治療を「継続」
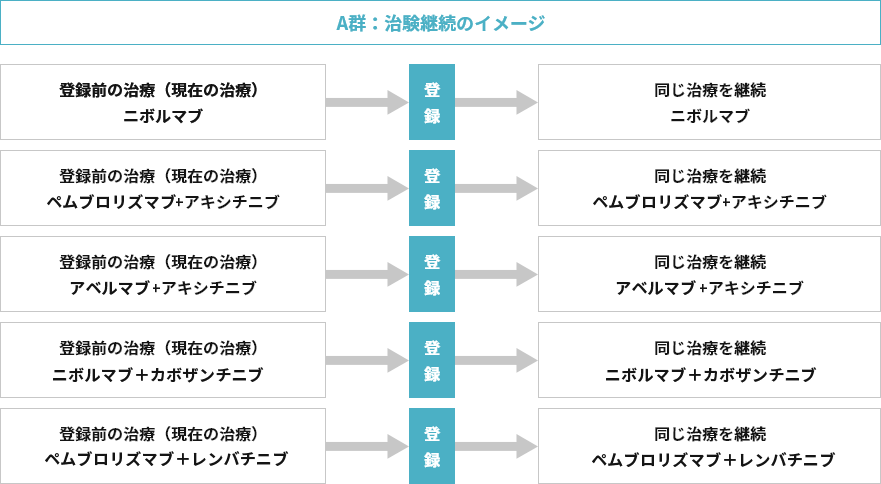
免疫チェックポイント阻害薬(ニボルマブ、ペムブロリズマブアベルマブ、アベルマブ)の治療を継続します。
- B群(試験治療)
- 現在受けている免疫チェックポイント阻害薬(ニボルマブ、ペムブロリズマブアベルマブ、アベルマブ)の治療を「休止」、
休止後増悪した場合は速やかに治療を再開します
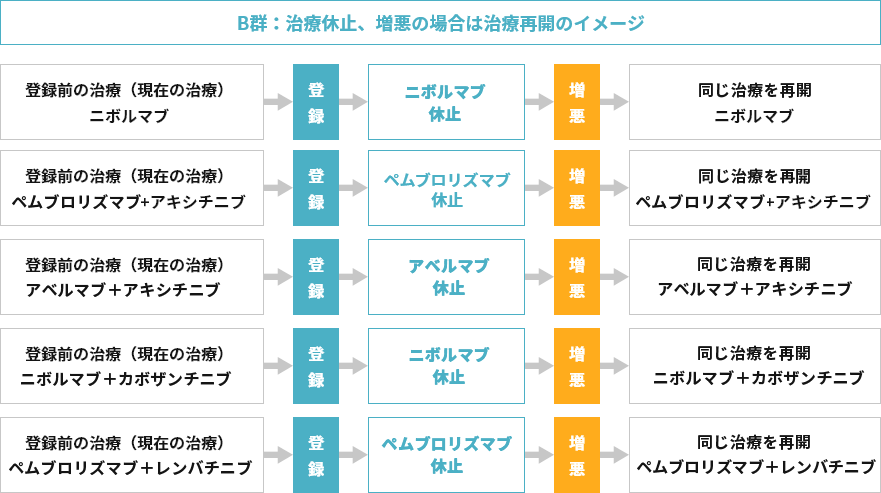
登録後、免疫チェックポイント阻害薬を休止します。休止中は、3~4週毎に外来を受診いただき、経過をみます。
ただし、現在ペムブロリズマブ+アキシチニブ、アベルマブ+アキシチニブの治療を受けている場合は、アキシチニブの内服を、
ニボルマブ+カボザンチニブの治療を受けている場合は、カボザンチニブの内服を、
ペムブロリズマブ+レンバチニブの治療を受けている場合は、レンバチニブの内服をそれぞれ継続します。
もし、休止をしている最中に病状が悪化してしまった場合には、すぐに免疫チェックポイント阻害薬による治療を再開します。
- 臨床試験参加への
ご相談・お問合せはこちら -
資料のダウンロードはこちら
本臨床試験紹介資料ダウンロード
臨床試験の参加について
臨床試験への登録
臨床試験への参加に同意されますと、担当医が臨床試験への登録を行い、治療が始まります。
正しい臨床試験の結果を得るため、登録後、A・Bどちらの治療法を受けていただくかはランダム(五分五分の確率)に決まります。この方法は治療法の比較において最も効果の高い方法と考えられており、世界中の臨床試験で採用されています。
- 登録から治療決定までの流れ
-
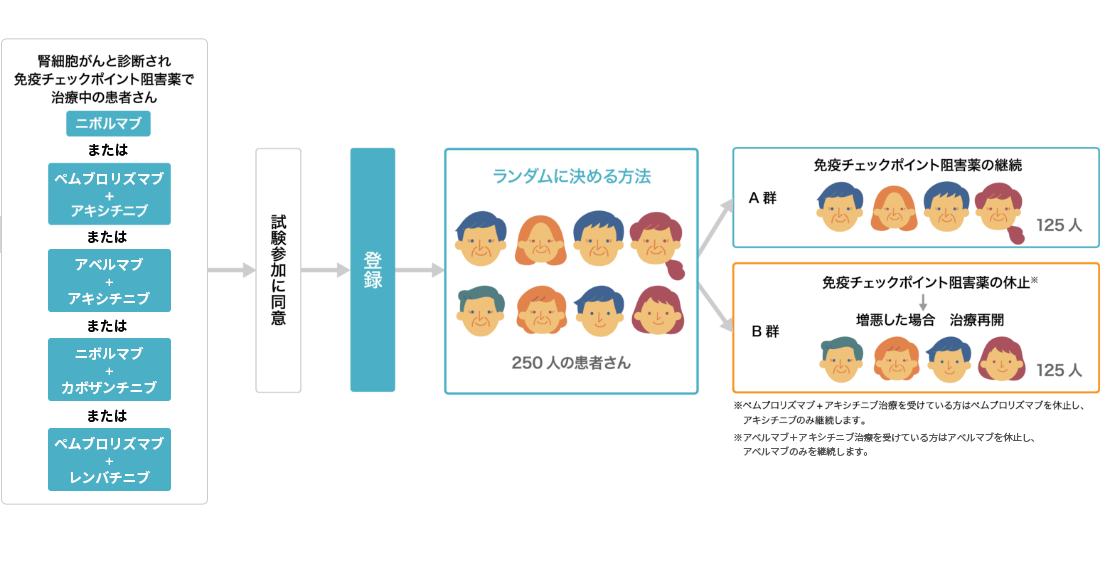
この臨床試験には250人の方にご協力いただく予定です。この臨床試験の予定期間は、研究開始日から2030年頃までの予定です。
臨床試験終了後の治療と進捗状況・結果について
臨床試験で行う治療が終了した後の治療については、終了時の身体の状態に合わせ、その時に最良と考えられる方法をご提案いたします。 また、この臨床試験の結果が判明し、いずれかの治療群が良いと結論された場合、もう一方の治療群に割り付けられた方につきましては、その時点の治療経過や身体の状態にあわせ、その時に最良と考えられる方法をご提案いたします。 進捗状況、主な結果はJCOGウェブサイト(www.jcog.jp)およびjRCTウェブサイト(https://jrct.niph.go.jp/)で公開しています。 公開はすべて個人を特定できない形で行われ、あなたの個人情報がこれらのウェブサイトに出ることはありません。
補償について
臨床試験で行う治療は、通常の診療の範囲内で行われ、用いる薬剤はいずれも保険診療で使用することができます。お見舞い金や各種手当てといった特別な経済的な補償は準備しておりません。
参加までの流れ
本臨床試験に関して、ご不明な点、医師、患者様に限らず、
九州大学泌尿器科研究事務局(TEL:092-642-5603)までお気軽にご相談、お問合せください。
-
1
- 担当医師より本臨床試験の説明
- 担当医師より臨床試験の説明を受けてください。

-
2
- 「同意書」のご記入
- 説明後、同意書の内容をご確認いただき、ご記入の上、担当医師にお渡しください。

-
3
- 検診(病院での)受診
- 病院にて検診を受診ください。

-
4
- 臨床試験参加
- 検診受診後、医師の指導のもと、臨床試験に参加いただきます。。

※最終的にご自身で選択し、決めていただくことになります。その結果、どのような決定をされたとしても、不利になるようなことはありません。
本試験に関するよくあるご質問
| Q. 休薬しても大丈夫ですか? |
|---|
| A. 休薬した患者さんも、病気が少しでも悪くなったら治療を再開します。見逃すことがないように、定期的に診察やCT 検査をします。休薬後に再開した場合でも、80%の患者さんに治療は有効と考えられています。( 治療を続けていても悪化する人がいるように、100%ではありません。) |
| Q. 医療費の負担は減りますか? |
|---|
| A. 薬剤費が大幅に減りますが、この研究に参加いただく方の負担は大きく変わらないことがあります。これは高額療養費制度にて、いままでかかっていた1 日当たり約3 ~ 4 万円の薬剤費の自己負担が大幅に軽減されていたからです。この研究で安全に休薬できることが分かれば、将来の患者さんだけでなく、またそれを支える社会的な負担も減らすことができます。 |
| Q. ランダム化比較試験とは? |
|---|
| A. 研究に参加していただけた場合、継続するのか、休薬するのかは「ランダム( 五分五分の確率で)」に決まります。あなたや担当医が治療法を選ぶと、元気な人や病変が小さい人だけに休薬してもらったりするなどで、患者さんの特徴に偏りが生じてしまう可能性があります。同じような病状の患者さんどうしで比べなければ、正しい試験の結果を得ることができません。治療法を比べるにはランダム化試験は最もよい方法と考えられおり、過去にあなたが受けていた治療もこのような研究に参加いただいた患者さんのおかげで有効であることが分かって、一般に使われるようになりました。 |
| Q. PD-1経路阻害薬で腎癌は治りますか? |
|---|
| A. PD-1経路阻害薬によって、がん細胞を攻撃する力( 免疫機能)が再活性化し、がん細胞が完全になくなったり、薬をやめた後も免疫機能が続いているために、病状が悪化しない人がいます。しかし残念ながら、治ったかどうかを証明できる検査はありません。薬物療法を続けている限りは治ったと言えないでしょうが、PD-1 経路阻害薬では治療をやめて5 年間以上再発しなければ、手術と同様に治ったと言える可能性があります。 |
| Q. この研究に参加すると、将来の医療がどう変わりますか? |
|---|
| A. PD-1 経路阻害薬の効果があった場合に、治療をやめても再発しない人がいます。ただ、いつ止めればよいか分からないので、副作用のために継続できなくなるまで、または効果がなくなるまで続けているのが現状です。この研究で、一度治療を休んでも効果が変わらないことがわかれば、将来の患者さんは副作用が出る前に休んだり、休んだまま効果が続いていれば治療を受けずに生活できる人が増えます。今後、PD-1経路阻害薬による治療を行う多くの腎細胞がんの患者さんや他の臓器のがん患者さんが治療を休むことで、副作用や医療費が抑えられるようになります。 |
本臨床試験責任者・連絡窓口
九州大学病院 泌尿器科 〒812-8582 福岡県福岡市東区馬出3-1-1 TEL:092-642-5603
- 研究事務局(臨床試験の実務責任者、連絡窓口)/ 研究代表医師(臨床試験全体の責任者):松元 崇
- 研究を統括する者:江藤 正俊
