医療分野におけるビッグデータ化がもたらすもの-医療情報データベース基盤整備事業「MID-NET®」とは

近年、医療分野のビッグデータ化が期待されています。医療分野において有効な情報を集め、それを分析することができれば、新薬や新しい治療法の発見など、患者さんにとってより有効な医療を提供することが可能となるからです。
なかでもPMDA(独立行政法人医薬品医療機器総合機構)による医療情報データベース基盤整備事業「MID-NET®」が、医療分野のビッグデータの一つとして注目を集めています。MID-NET®とは、全国の協力医療機関(10拠点23病院)の電子カルテ等の病院情報システムに含まれる情報を、個人情報に配慮しながら、統合解析することができるデータベースシステムの名称です。
MID-NET®はもともと医薬品等の安全対策を推進するために誕生しましたが、有効性の評価等への利活用にも期待が集まっています。2018年度の運用開始に向けて、現在はシステムの検証作業と利活用のルール等を検討している段階だといいます。今回は、PMDAの理事長であり、JUMP理事・電子診療情報活用検証PJ委員会委員長でもある近藤 達也先生に、MID-NET®による効果や今後の展望についてお話をお伺いしました。
これまで医療情報は個別管理されてきた
これまで、医療情報は病院ごとの個別管理が当たり前でした。そのため、医療情報をひとつのデータベースに集約することは困難とされてきました。

しかし近年はより効率的で効果的な医療を目指すため、医療情報のビッグデータ化が進行しています。そのひとつが「MID-NET®」です。
ビッグデータの鍵となる医療情報データベース基盤整備事業「MID-NET®」とは
MID-NET®とは、厚生労働省が公募により選定した協力医療機関(10拠点23病院)を拠点とした分散型のデータベース分析システムです。各協力医療機関が独自で保有している病院情報システムから、傷病情報、処方情報、検査結果情報等の情報を標準化データベースに格納し、適切な匿名化処理を実施した上で各拠点に集積されています。データを分析する時は、専用回線を通じて複数拠点のデータを統合解析することが可能です。
本事業において、PMDAは協力医療機関のシステム構築を担うと共に、分析システムを構築しており、安全対策への利用を念頭に、この医療情報データベースの試行的利活用を開始しています。MID-NET®は、国費と製薬企業からの安全対策拠出金を財源として、2012年度から厚生労働省の事業として開始し、2018年度に本格稼働する予定となっています。
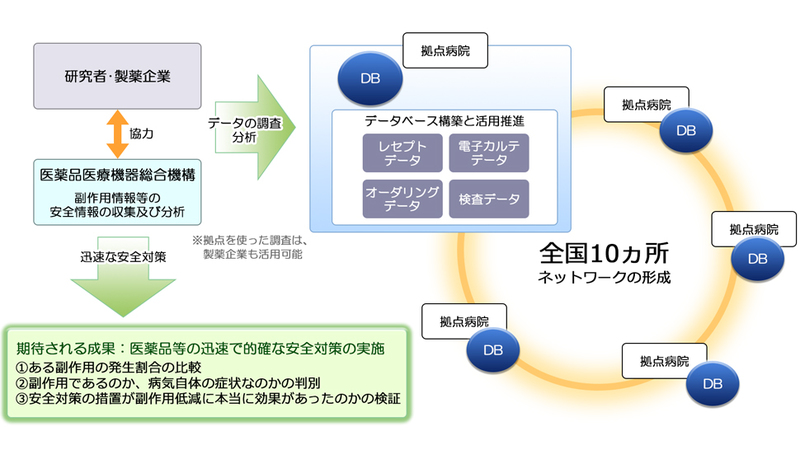
全国に広がる10拠点23病院がネットワークの拠点となります。各拠点で管理されているデータベースはネットワーク化され、ビッグデータとして医薬品等の安全対策などに一定の効果をあげることが期待されています。
MID-NET®が誕生した背景―きっかけは薬害事件
MID-NET®はもともと医薬品の安全対策として誕生した
かつて、薬事の世界では薬害が大きな問題となっていました。薬害とは、医薬品による健康被害が生じた際に行政的な対応の遅れが原因で病気が悪化し、救えるべき患者さんを救えない事例を指します。たとえば、1960年代から問題となった薬害肝炎事件では、行政の対応が遅れたために多くの方がC型肝炎ウイルスに感染しました。
これまでの安全対策は、主として製造販売業者や医療関係者からの個別の副作用報告に基づき実施してきましたが、規制当局自らが情報を分析し、安全対策の必要性を判断し対応する必要があると考えられるようになりました。
このような考えのもと、MID-NET®は規制当局が主体的にデータを集め医薬品の安全対策に生かすために誕生しました。
MID-NET®のデータはどのくらい集まっているのか
現在のところ、データの数は400万人程度ですが、最終的には1000万人規模のデータを目指しています。
新薬の開発
現在、日本の新薬の審査は世界一のスピードを誇っています。それは、医薬品等の審査を行う我々PMDAも、企業や研究者を対象に薬事戦略相談などを実施し、有望なシーズ(種)を開発の次段階に結びつけるための支援を行っており、実用化に向けての課題を開発の早期から把握し、助言を実施しているからです。
日本は薬のシーズを持つ企業も多く、新薬の開発に非常に熱心です。しかし、規制への理解が不足していることなどが原因で、基礎研究から実用化への障壁を乗り越えることが難しかった現状があります。これを解消するため、PMDAは薬事戦略相談等を通じ、開発初期から必要な試験・治験に関する指導・助言を行うことで、より安全で効果的な医薬品の開発促進に寄与していいます。
MID-NET®で集められたデータは、新薬を開発する研究者や製薬企業にとっても非常に有用なデータとなるでしょう。リアルタイムでデータを入手し、それをもとに調査や分析ができるようになれば、新薬の開発のスピードも上がることが期待されます。
医薬品の市販後調査
医薬品は通常、臨床試験を経て、有効性・安全性・品質の厳格な審査のもとで使用が承認されます。しかし、臨床試験で得られる安全性の情報には限界があります。
たとえば販売開始後、様々な背景を持つ患者さんが医薬品を使用した結果、稀に重篤な副作用が起こると判明する場合があります。
現在の副作用報告制度には主に下記のような課題があります。
・医師等の医療関係者からの自発的な報告であるため、報告がなされなければ副作用の発生がわからないこと
・自発報告であることから、他剤との副作用発生頻度を単純に比較することができないこと
・原疾患による症状と副作用なのか判断が難しいこと
MID-NET®のデータを活用すると、医療関係者からの副作用報告を待つことなく、データベースを利用してリアルタイムに副作用の発生状況等が調査できるようになります。また、同種同効果の他剤との副作用の発現頻度の比較も実施可能となります。このように、これまでの副作用報告制度における課題がMID-NET®の稼働により解決できると考えられています。
MID-NET®の課題は情報や医療機関が限定されていること
お話してきたように非常に有用なMID-NET®ですが、いくつかの課題もみえてきています。まず、現状集めることができるデータは入院期間の情報となるので、主に急性期の薬の反応についてはカバーできますが、来院前や転院後の情報とひも付けることはできません。これは今後解決が必要となる課題のひとつとされています。

また、現在はネットワークの対象となる医療機関が限られていることもひとつの課題です。
今後MID-NET®のネットワークに参画する医療機関を増やしていくためには、MID-NET®の有用性を広く周知し、理解いただくことで他の医療機関も参画したいと思う仕組み作りが重要であると考えています。
現在、多くの病院は情報共有の認識が不足しており、自分の病院の情報管理のみを優先して考えているという現状があります。MID-NET®に参画していない医療機関にも、病院同士のネットワークが重要であると理解してもらう活動が必要となるでしょう。
MID-NET®は徹底した安全管理の元で運営する必要がある

お話してきたような医療情報をビッグデータ化するうえで、国民や企業に不安を与えることがあってはならないと考えています。たとえば個人情報の漏えいは絶対に防止しなければならず、きちんとしたルールを作り、徹底した安全管理の中で運営することが非常に重要になります。我々は、国民の方々に「MID-NET®に加入している病院は安全対策がきちんとなされており、安心して診療を受けることができる」と判断される運営体制を目指しています。
医師の方へ
様々な学会と連携し、日々の診療・研究に役立つ医師向けウェビナーを定期配信しています。
情報アップデートの場としてぜひご視聴ください。
